Ochrona patentowa leków to niezwykle istotny aspekt rynku farmaceutycznego, mający bezpośredni wpływ na dostępność innowacyjnych terapii i ich ceny. Zrozumienie, jak długo trwa taka ochrona w Polsce, jest kluczowe nie tylko dla producentów, ale także dla pacjentów i całego systemu ochrony zdrowia. Pozwala to ocenić, kiedy można spodziewać się pojawienia się tańszych zamienników.
Ochrona patentowa leków w Polsce trwa 20 lat, z możliwością przedłużenia do 25 lat
- Podstawowy okres ochrony patentowej na lek wynosi 20 lat, liczony od daty zgłoszenia wynalazku w Urzędzie Patentowym.
- Możliwe jest uzyskanie Dodatkowego Prawa Ochronnego (SPC), które może wydłużyć ochronę maksymalnie o 5 lat.
- Całkowity okres ochrony od momentu dopuszczenia leku do obrotu nie może przekroczyć 15 lat.
- Oprócz patentu, leki oryginalne korzystają z wyłączności danych regulacyjnych, najczęściej w formule "8+2+1".
- Leki generyczne mogą wejść na rynek dopiero po wygaśnięciu wszystkich form ochrony.
Ile lat trwa ochrona patentowa na lek? Kluczowe informacje
Podstawowy okres ochrony patentowej na lek w Polsce wynosi standardowo 20 lat. Jest to ogólny czas trwania patentu na wynalazek, zgodny z polskim prawem własności przemysłowej. Ta 20-letnia ochrona ma na celu zapewnienie wynalazcy wyłączności w korzystaniu z jego pomysłu przez znaczący okres, co ma zachęcać do ponoszenia ryzyka i kosztów związanych z badaniami i rozwojem.
Od kiedy zegar zaczyna tykać? Wyjaśniamy moment startowy
Kluczową informacją, którą należy zapamiętać, jest to, że 20-letni okres ochrony patentowej liczy się od daty zgłoszenia wynalazku w Urzędzie Patentowym. Nie jest to więc czas od momentu, gdy lek trafia do aptek czy szpitali, ale od momentu złożenia wniosku o patent. Ta różnica w punktach startowych jest fundamentalna dla zrozumienia całego mechanizmu ochrony i późniejszego wprowadzania leków generycznych.
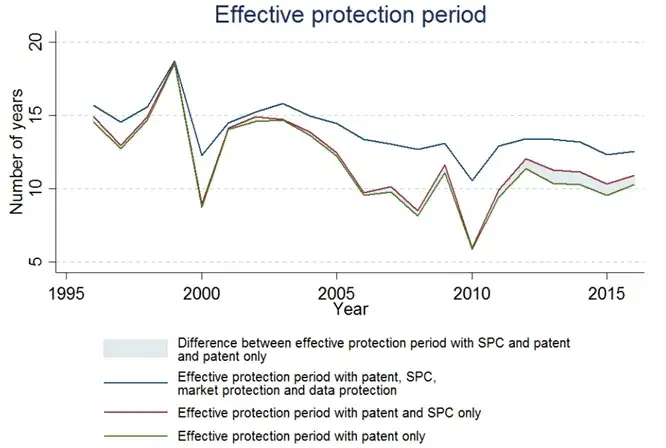
Czy 20 lat to ostateczny termin? Dodatkowe Prawo Ochronne (SPC)
Choć 20 lat to podstawowy okres ochrony patentowej, w przypadku produktów leczniczych istnieje mechanizm, który pozwala na jego przedłużenie. Jest to tzw. Dodatkowe Prawo Ochronne (SPC - Supplementary Protection Certificate). Nie jest to nowy patent, ale rozszerzenie ochrony wynikającej z istniejącego patentu, specjalnie dedykowane dla leków.
Czym jest SPC i dlaczego powstało? Rekompensata za lata badań
Dodatkowe Prawo Ochronne (SPC) zostało wprowadzone jako sposób na zrekompensowanie producentom leków czasu, który tracą na długotrwałe badania kliniczne i procedury rejestracyjne. Zanim lek uzyska pozwolenie na dopuszczenie do obrotu, mija często wiele lat od daty zgłoszenia patentowego. SPC ma więc na celu przywrócenie producentowi części utraconego okresu wyłączności, który mógłby efektywnie wykorzystać na komercjalizację swojego innowacyjnego produktu.
O ile maksymalnie można wydłużyć patent? Konkretne ramy czasowe
Dodatkowe Prawo Ochronne może przedłużyć ochronę patentową maksymalnie o 5 lat. Należy jednak pamiętać o pewnym ograniczeniu: całkowity okres ochrony od momentu dopuszczenia leku do obrotu nie może przekroczyć 15 lat. Oznacza to, że nawet jeśli patent był złożony bardzo wcześnie, a lek długo czekał na rejestrację, okres jego wyłączności po dopuszczeniu do obrotu jest limitowany.
Patent to nie wszystko: Wyłączność danych i jej znaczenie
Oprócz ochrony patentowej, oryginalne produkty lecznicze korzystają z jeszcze jednej, bardzo istotnej formy ochrony, zwanej wyłącznością danych regulacyjnych. Jest to mechanizm niezależny od patentu, który chroni dokumentację badawczą i kliniczną leku. Wyłączność danych uniemożliwia firmom generycznym powoływanie się na badania przeprowadzone przez producenta leku oryginalnego przy składaniu własnych wniosków rejestracyjnych.
Formuła "8+2+1": Jak działa niewidzialna tarcza dla leków oryginalnych
W Unii Europejskiej, w tym w Polsce, wyłączność danych regulacyjnych najczęściej funkcjonuje w oparciu o tzw. formułę "8+2+1". Oto jak to działa:
- Przez pierwsze 8 lat od daty dopuszczenia leku oryginalnego do obrotu, firmy produkujące leki generyczne nie mogą wykorzystywać jego danych rejestracyjnych do uzyskania własnego pozwolenia na dopuszczenie do obrotu.
- Po upływie tych 8 lat, firma generyczna może złożyć wniosek o rejestrację swojego leku. Jednakże, zgodnie z zasadą "8+2", może ona wprowadzić swój produkt na rynek dopiero po upływie łącznie 10 lat od daty dopuszczenia do obrotu leku oryginalnego.
- Istnieje możliwość przedłużenia tego okresu o dodatkowy rok (formuła "8+2+1"). Dzieje się tak, jeśli producent leku oryginalnego w ciągu pierwszych 8 lat od dopuszczenia do obrotu zarejestruje nowe, istotne wskazanie terapeutyczne dla swojego produktu.
Warto również wspomnieć o specjalnych regulacjach dotyczących leków sierocych, które są stosowane w leczeniu rzadkich chorób. W Unii Europejskiej takie leki uzyskują 10-letni okres wyłączności rynkowej od momentu dopuszczenia do obrotu, co ma na celu zachęcenie do ich rozwoju.
Różnica między patentem a wyłącznością danych kluczowe rozróżnienie
Choć oba mechanizmy służą ochronie innowacyjnych leków, patent i wyłączność danych regulacyjnych to dwie różne rzeczy. Patent chroni sam wynalazek czyli nową substancję czynną, sposób jej wytwarzania lub zastosowanie. Chroni go przed kopiowaniem przez konkurencję. Z kolei wyłączność danych chroni dokumentację dotyczącą bezpieczeństwa i skuteczności leku, która została złożona w procesie rejestracyjnym. Patent liczy się od daty zgłoszenia, a wyłączność danych od daty dopuszczenia leku do obrotu. Oba te okresy mogą się nakładać, ale ich punkty startowe i czas trwania są odrębne.
Linia czasu ochrony leku: Od laboratorium do apteki
Aby lepiej zobrazować, jak poszczególne etapy ochrony wpływają na dostępność leków, warto przedstawić je w formie chronologicznej linii czasu. Jest to proces wieloetapowy, w którym różne formy ochrony przeplatają się i uzupełniają.
Krok 1: Zgłoszenie patentowe początek 20-letniej ochrony
Wszystko zaczyna się od zgłoszenia patentowego. Jest to moment, w którym wynalazca składa wniosek o ochronę swojego innowacyjnego rozwiązania w Urzędzie Patentowym. Od tej daty rozpoczyna się bieg 20-letniego okresu ochrony patentowej. Nawet jeśli proces uzyskiwania patentu trwa kilka lat, punktem wyjścia jest zawsze data pierwotnego zgłoszenia.
Krok 2: Dopuszczenie do obrotu start dla wyłączności danych
Po przejściu przez rygorystyczne badania kliniczne i proces rejestracyjny, lek otrzymuje pozwolenie na dopuszczenie do obrotu. Jest to kluczowy moment, ponieważ właśnie od tej daty zaczyna biec okres wyłączności danych regulacyjnych, najczęściej w formule "8+2" lub "8+2+1". Jest to również moment, od którego liczy się potencjalny okres 15 lat maksymalnej ochrony od dopuszczenia do obrotu.
Krok 3: Złożenie wniosku o SPC walka o dodatkowe 5 lat
W odpowiednim momencie, zazwyczaj po uzyskaniu pozwolenia na dopuszczenie do obrotu, producent leku oryginalnego może złożyć wniosek o przyznanie Dodatkowego Prawa Ochronnego (SPC). Celem jest uzyskanie maksymalnie 5 dodatkowych lat ochrony patentowej, które zrekompensują czas stracony na procedury administracyjne. SPC jest przyznawane przez odpowiedni urząd, na podstawie spełnienia określonych warunków.
Krok 4: Wygaśnięcie ochrony zielone światło dla leków generycznych
Dopiero gdy wygasną wszystkie formy ochrony zarówno podstawowy patent, jak i ewentualne Dodatkowe Prawo Ochronne (SPC), a także okresy wyłączności danych regulacyjnych rynek otwiera się na konkurencję. Jest to moment, w którym firmy produkujące leki generyczne mogą legalnie wprowadzić na rynek swoje zamienniki, korzystając z już opracowanych i potwierdzonych danych.
Co się dzieje, gdy ochrona leku wygasa? Era generyków
Wygaśnięcie ochrony patentowej i innych form wyłączności to przełomowy moment dla rynku farmaceutycznego i dla pacjentów. Otwiera drzwi dla konkurencji, która może znacząco wpłynąć na ceny i dostępność leków.
Jak wygaśnięcie patentu otwiera rynek dla tańszych zamienników?
Gdy patent na lek wygasa, a wraz z nim kończy się okres wyłączności danych i ewentualne SPC, producenci leków generycznych mogą rozpocząć produkcję i sprzedaż swoich wersji leku. Ponieważ firmy generyczne nie ponoszą kosztów związanych z pierwotnymi badaniami i rozwojem, mogą zaoferować swoje produkty po znacznie niższych cenach. Prowadzi to do zwiększonej konkurencji na rynku, co jest korzystne dla konsumentów.
Przeczytaj również: Ból dziąseł? Szybka ulga: domowe sposoby i apteka
Korzyści dla pacjentów i systemu ochrony zdrowia
Wejście na rynek leków generycznych po wygaśnięciu ochrony przynosi szereg istotnych korzyści:
- Znaczące obniżenie cen leków często nawet o kilkadziesiąt procent w porównaniu do ceny leku oryginalnego.
- Zwiększenie dostępności terapii dla większej liczby pacjentów, którzy wcześniej mogli nie być w stanie pozwolić sobie na droższe leki.
- Oszczędności dla systemu ochrony zdrowia niższe ceny leków oznaczają mniejsze wydatki dla budżetu państwa, NFZ oraz dla samych pacjentów ponoszących koszty leczenia.

